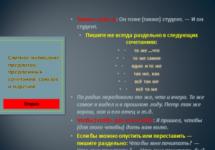
Положение элементов-неметаллов в Периодической системе химических элементов Д.И. Менделеева
· Элементы-неметаллы:
· s-элемент – водород;
· р-элементы 3 группы – бор;
· 4 группы – углерод и кремний;
· 5 группы – азот, фосфор и мышьяк,
· 6 группы – кислород, сера, селен и теллур
· 7 группы – фтор, хлор, бром, йод и астат.
Элементы 8 группы – инертные газы, занимают особое положение, они имеют полностью завершенный внешний электронный слой.
Химические элементы-неметаллы могут проявлять как окислительные, так и восстановительные свойства, в зависимости от химического превращения, в котором они принимают участие.
Атомы самого электроотрицательного элемента – фтора – не способны отдавать электроны, он всегда проявляет только окислительные свойства, другие элементы могут проявлять и восстановительные свойства, хотя намного в меньшей степени, чем металлы. Наиболее сильными окислителями (принимают электроны) - являются фтор, кислород и хлор, преимущественно восстановительные свойства (отдают) проявляют водород, бор, углерод, кремний, фосфор, мышьяк и теллур. Промежуточные окислительно-восстановительные свойства имеют азот, сера, йод.
1. Взаимодействие с металлами:
2Na + Cl 2 = 2NaCl, Fe + S = FeS, 6Li + N 2 = 2Li 3 N, 2Ca + O 2 = 2CaO
в этих случаях неметаллы проявляют окислительные свойства, они принимают электроны, образуя отрицательно заряженные частицы.
2. Взаимодействие с другими неметаллами:
· взаимодействуя с водородом , большинство неметаллов проявляет окислительные свойства, образуя летучие водородные соединения – ковалентные гидриды:
3H 2 + N 2 = 2NH 3 , H 2 + Br 2 = 2HBr;
· взаимодействуя с кислородом , все неметаллы, кроме фтора, проявляют восстановительные свойства:
S + O 2 = SO 2 , 4P + 5O 2 = 2P 2 O 5 ;
· при взаимодействии с фтором фтор является окислителем, а кислород – восстановителем: 2F 2 + O 2 = 2OF 2 ;
· неметаллы взаимодействуют между собой , более электроотрицательный металл играет роль окислителя, менее электроотрицательный – роль восстановителя: S + 3F 2 = SF 6 , C + 2Cl 2 = CCl 4 .
Галогены (7 группа)
Химические свойства галогенов.
КИСЛОРОДСОДЕРЖАЩИЕ КИСЛОТЫ ХЛОРА
· Хлорноватистая кислота HCl +1 O соли – гипохлориты
Существует только в виде разбавленных водных растворов.
Получение Cl2 + H2O = HCl + HClO
Химические свойства
HClO - слабая кислота и сильный окислитель:
1) Разлагается на свету, выделяя атомарный кислород HClO = HCl + O
2) Со щелочами дает соли – гипохлориты HClO + KOH = KClO + H2O
3) Взаимодействует с галогеноводородами 2HI + HClO = I2 + HCl + H2O
Хлористая кислота HClO2 (HClO2 - слабая кислота и сильный окислитель; соли хлористой кислоты – хлориты)
Химические свойства
1.HClO2 + KOH = KClO2 + H2O
2. Неустойчива, при хранении разлагается 4HClO2 = HCl + HClO3 + 2ClO2 + H2O
Хлорноватая кислота HCl O3 (HClO3 - Сильная кислота и сильный окислитель; соли хлорноватой кислоты – хлораты)
KClO 3 - Бертоллетова соль ; ее получают при пропускании хлора через подогретый (40°C) раствор KOH:
3Cl 2 + 6KOH = 5KCl + KClO 3 + 3H 2 O
Бертоллетову соль используют в качестве окислителя; при нагревании она разлагается:
4KClO 3 = KCl + 3KClO 4 (без катализатора)
2KClO 3 = 2KCl + 3O 2 (катализатор MnO 2)
Хлорная кислота HClO4 (HClO4 - очень сильная кислота и очень сильный окислитель; соли хлорной кислоты – перхлораты )
Получение KClO4 + H2SO4 = KHSO4 + HClO4
Химические свойства
1) Взаимодействует со щелочами HClO4 + KOH = KClO4 + H2O
2) При нагревании хлорная кислота и ее соли разлагаются:
4HClO4 = 4ClO2 + 3O2 + 2H2O KClO4 = KCl + 2O2
Халькогены (элементы VIA группы)
Кислород, S, Se, Te, Po. Название халькогены означает «рождающие руды». Соединения серы: пирит, или железный колчедан – FeS2, киноварь – HgS, цинковая обманка – ZnS.
На внешнем энергетическом уровне у халькогенов 6 электронов. До завершения внешнего энергетического уровня атомам не хватает 2 электрона, поэтому они присоединяют электроны и проявляют в своих соединениях степень окисления -2.
Атомы серы, селена и теллура в своих соединениях с более электроотрицательными элементами проявляют положительные степени окисления +2, +4 и +6.
Кислород n=8 1s 2 2s 2 2p 4
Кислород входит в состав таких руд, как корунд – Al2O3, магнитный железняк, – Fe3O4, красный железняк – Fe2O3, бурый железняк - Fe2O3 ·
Кислород в соединении с фтором – OF2 проявляет степень окисления +2. Кислород входит в состав атмосферы, где на его долю приходится 21%.
Получение кислорода.
· В промышленности кислород получают из жидкого воздуха.
· Кислород можно получить и при разложении воды в специальном устройстве – электролизёре.

· В лаборатории используют пероксид водорода (Н2О2). Эта реакция идёт в присутствии катализатора – оксида марганца IV
![]()
· в лаборатории ещё используют реакцию разложения перманганата калия – KMnO 4 – «марганцовки».

· В лабораторных условиях кислород выделяется кислород при нагревании бертолетовой соли (хлората калия)
2KClO 3 = 2KCl + 3O 2 Катализатор - оксид марганца (MnO 2).
кислород существует в виде двух аллотропных модификаций –O 2 и О 3 .
Химические свойства
Кислород не взаимодействует с галогенами, благородными газами, золотом и платиной.
· Кислород энергично реагирует с металлами. Например, в реакции с литием, образуется оксид лития, в реакции с медью – оксид меди (II).
4Li + O 2 = 2Li 2 O 2Cu + O 2 = 2CuO
· Кислород реагирует с неметаллами.
S + O 2 = SO 2 4P + 5O 2 = 2P 2 O 5
Почти все реакции с кислородом экзотермические (то есть сопровождаются выделением теплоты). Исключение составляет реакция азота с кислородом, которая является эндотермической.
N 2 + O 2 ↔ 2NO – Q
· Кислород сложные вещества.
CH 4 + 2O 2 = CO 2 + 2H 2 O 2H 2 S + 3O 2 = 2SO 2 + 2H 2 O
СЕРА n=16 1s 2 2s 2 2p 6 3s 2 3p 4
1. Металлы реагируют с неметаллами.
2 Me + n Hal 2 → 2 MeHal n
4Li + O2 = 2Li2O
Щелочные металлы, за исключением лития, образуют пероксиды:
2Na + O 2 = Na 2 O 2
2. Металлы, стоящие до водорода, реагируют с кислотами (кроме азотной и серной конц.) с выделением водорода
Me + HCl → соль + H2
2 Al + 6 HCl → 2 AlCl3 + 3 H2
Pb + 2 HCl → PbCl2↓ + H2
3. Активные металлы реагируют с водой с образованием щелочи и выделением водорода.
2Me + 2n H 2 O → 2Me(OH) n + n H 2
Продуктом окисления металла является его гидроксид – Me(OH) n (где n-степень окисления металла).
Например:
Ca + 2H 2 O → Ca(OH) 2 + H 2
4. Металлы средней активности реагируют с водой при нагревании, образуя оксид металла и водород.
2Me + nH 2 O → Me 2 O n + nH 2
Продукт окисления в таких реакциях – оксид металла Me 2 O n (где n-степень окисления металла).
3Fe + 4H 2 O → Fe 2 O 3 ·FeO + 4H 2
5. Металлы, стоящие после водорода, с водой и растворами кислот (кроме азотной и серной конц.) не реагируют
6. Более активные металлы вытесняют менее активные из растворов их солей.
CuSO 4 + Zn = Zn SO 4 + Cu
CuSO 4 + Fe = Fe SO 4 + Cu
Активные металлы ‑ цинк и железо заместили медь в сульфате и образовали соли. Цинк и железо окислились, а медь восстановилась.
7. Галогены реагируют с водой и раствором щелочи.
Фтор в отличие от других галогенов воду окисляет:
2H 2 O + 2F 2 = 4HF + O 2 .
на холоде: Cl2+2KOH=KClO+KCl+H2OCl2+2KOH=KClO+KCl+H2O образуется хлорид и гипохлорит
при нагревании: 3Cl2+6KOH−→KClO3+5KCl+3H2O3Cl2+6KOH→t,∘CKClO3+5KCl+3H2O образуется лорид и хлорат
8 Активные галогены (кроме фтора) вытесняют менее активные галогены из растворов их солей.
9. Галогены не реагируют с кислородом.
10. Амфотерные металлы (Al, Be, Zn) реагируют с растворами щелочей и кислот.
3Zn+4H2SO4=3 ZnSO4+S+4H2O
11. Магний реагирует с углекислым газом и оксидом кремния.
2Мg + CO2 = C + 2MgO
SiO2+2Mg=Si+2MgO
12. Щелочные металлы (кроме лития) с кислородом образуют пероксиды.
2Na + O 2 = Na 2 O 2
3. Классификация неорганических соединений
Простые вещества – вещества, молекулы которых состоят из атомов одного вида (атомов одного элемента). В химических реакциях не могут разлагаться с образованием других веществ.
Сложные вещества (или химические соединения) – вещества, молекулы которых состоят из атомов разного вида (атомов различных химических элементов). В химических реакциях разлагаются с образованием нескольких других веществ.
Простые вещества разбиваются на две большие группы: металлы и неметаллы.
Металлы – группа элементов, обладающая характерными металлическими свойствами: твёрдые вещества (исключение составляет ртуть) имеют металлический блеск, являются хорошими проводниками теплоты и электричества, ковкие (железо (Fe), медь (Cu), алюминий (Al), ртуть (Hg), золото (Au), серебро (Ag) и др.).
Неметаллы – группа элементов: твёрдые, жидкие (бром) и газообразные веществ, которые не обладают металлическим блеском, являются изоляторы, хрупкие.
А сложные вещества в свою очередь подразделятся на четыре группы, или класса: оксиды, основания, кислоты и соли.
Оксиды – это сложные вещества, в состав молекул которых входят атомы кислорода и какого – нибудь другого вещества.
Основания – это сложные вещества, в которых атомы металлов соединены с одной или несколькими гидроксильными группами.
С точки зрения теории электролитической диссоциации, основания – сложные вещества, при диссоциации которых в водном растворе образуются катионы металла (или NH4+) и гидроксид – анионы OH-.
Кислоты – это сложные вещества, в состав молекул которых входят атомы водорода, способные замещаться или обмениваться на атомы металла.
Соли – это сложные вещества, молекулы которых состоят из атомов металлов и кислотных остатков. Соль представляет собой продукт частичного или полного замещения атомов водорода кислоты металлом.
Лекция 24
Неметаллы.
План лекции:
Неметаллы – простые вещества
Положение неметаллов в периодической системе
Число элементов-неметаллов значительно меньше, чем элементов-металлов Типичными неметаллическими свойствами обладают десять химических элементов (Н, С, N, Р, О, S, F, Cl, Br, I). Шесть элементов, которые обычно относят к неметаллам, проявляют двойственные (и металлические, и неметаллические) свойства (В, Si, As, Se, Те, At). И еще 6 элементов в последнее время стали включать в список неметаллов. Это так называемые благородные (или инертные) газы (Не, Ne, Аг, Кг, Хе, Rn). Итак, 22 из известных химических элементов принято относить к неметаллам.
Элементы, проявляющие неметаллические свойства в периодической системе располагаются выше диагонали бор-астат (рис. 26).
Атомы большинства неметаллов, в отличие от атомов металлов, на внешнем электронном слое имеют большое число электронов - от 4 до 8. Исключение составляют атомы водорода, гелия, бора, которые имеют на внешнем уровне 1, 2 и 3 электрона соответственно.
Среди неметаллов только два элемента - водород (1s 1) и гелий (1s 2) относятся к s-семейству, все остальные принадлежат к р -семейству.
Атомы типичных неметаллов (A) характеризуются высокой электроотрицательностью и большим сродством к электрону, что обусловливает их способность образовывать отрицательно заряженные ионы с электронными конфигурациями соответствующих инертных газов:
А 0 + nê → А n -
Эти ионы входят в состав ионных соединений неметаллов с типичными металлами. Отрицательные степени окисления неметаллы имеют также в ковалентных соединениях с другими менее электроотрицательными неметаллами (в частности, с водородом).
Атомы неметаллов в ковалентных соединениях с более электроотрицательными неметаллами (в частности, с кислородом) имеют положительные степени окисления. Высшая положительная степень окисления неметалла , как правило, равна номеру группы , в которой он находится.
Неметаллы – простые вещества
Несмотря на небольшое число элементов-неметаллов, их роль и значение как на Земле, так и в космосе огромны. 99% массы Солнца и других звезд составляют неметаллы водород и гелий. Воздушная оболочка Земли состоит из атомов неметаллов - азота, кислорода и благородных газов. Гидросфера Земли образована одним из важнейших для жизни веществ - водой, молекулы которой состоят из неметаллов водорода и кислорода. В живой материи главенствуют 6 неметаллов - углерод, кислород, водород, азот, фосфор, сера.
При обычных условиях вещества-неметаллы существуют в разных агрегатных состояниях:
1) газы: водород Н 2 , кислород О 2 , азот N 2 , фтор F 2 , хлор С1 2 , инертные газы: Не, Ne, Ar, Кг, Хе, Rn
2) жидкости: бром Вг 2
3) твердые вещества йод I 2 , углерод С, кремний Si, сера S, фосфор Р и др.
Семь элементов-неметаллов образуют простые вещества, существующие в виде двухатомных молекул Э 2 (водород Н 2 , кислород О 2 , азот N 2, фтор F 2 , хлор С1 2 , бром Вг 2, йод I 2) .
Так как в кристаллической решетке неметаллов между атомами нет свободных электронов, они отличаются по физическим свойствам от металлов:
¾ не имеют блеска;
¾ хрупкие, имеют различную твердость;
¾ плохо проводят тепло и электричество.
Твердые вещества-неметаллы в воде практически нерастворимы; газообразные О 2 , N 2 , Н 2 и галогены обладают очень малой растворимостью в воде.
Для ряда неметаллов характерна аллотропия - явление существование одного элемента в виде нескольких простых веществ. Аллотропные модификации известны для кислорода (кислород О 2 и озон О 3), серы (ромбическая, моноклинная и пластическая), фосфора (белый, красный и черный), углерода (графит, алмаз и карбин и др.), кремния (кристаллический и аморфный).
Химические свойства неметаллов
По химической активности неметаллы существенно различаются между собой. Так, азот и благородные газы, в химические реакции вступают только при очень жестких условиях (высокое давление и температура, наличие катализатора).
Наиболее химически активными неметаллами являются галогены, водород и кислород. Сера, фосфор, а особенно углерод и кремний реакционноспособны только при повышенных температурах.
Неметаллы в химических реакциях проявляют и окислительные, и восстановительные свойства. Наиболее высокая окислительная способность характерна для галогенов и кислорода. У таких неметаллов, как водород, углерод, кремний, преобладают восстановительные свойства.
I. Окислительные свойства неметаллов:
1. Взаимодействие с металлами. При этом образуются бинарные соединения: с кислородом – оксиды, с водородом – гидриды, азотом – нитриды, галогенами – галогениды и т.д.:
2Cu + O 2 → 2CuO
2Fe + 3Cl 2 → 2FeCl 3
2. Взаимодействие с водородом. Неметаллы выступают в качестве окислителей и в реакциях с водородом, образуя при этом летучие водородные соединения:
Н 2 + С1 2 → 2НС1
N 2 + 3Н 2 → t, p, кат. 2NH 3
3. Взаимодействие с неметаллами. Неметаллы проявляют окислительные свойства также в реакциях с менее электроотрицательными неметаллами:
2Р + 5С1 2 → 2РС1 5 ;
С + 2S → CS 2 .
4. Взаимодействие со сложными веществами. Окислительные свойства неметаллов могут проявляться и в реакциях со сложными веществами. Например, вода горит в атмосфере фтора:
2F 2 + 2Н 2 О → 4HF + О 2 .
II. Восстановительные свойства неметаллов
1. Взаимодействие с неметаллами . Восстановительные свойства неметаллы могут проявлять по отношению к неметаллам с большей электроотрицательностью, и в первую очередь по отношению к фтору и кислороду:
4Р + 5О 2 → 2Р 2 О 5 ;
N 2 + О 2 → 2NO
2. Взаимодействие со сложными веществами. Некоторые неметаллы могут являться восстановителями, что позволяет применять их в металлургическом производстве:
С + ZnO → Zn + СО;
5Н 2 + V 2 О 5 → 2V + 5Н 2 О.
SiО 2 + 2С → Si + 2СО.
Восстановительные свойства неметаллы проявляют при взаимодействии со сложными веществами - сильными окислителями, например:
3S + 2КСlO 3 → 3SO 2 + 2КС1;
6Р + 5КСlO 3 → ЗР 2 O 5 + 5КС1.
С + 2H 2 SО 4 → СО 2 + 2SО 2 + 2Н 2 О;
3Р + 5HNО 3 + 2Н 2 О → ЗН 3 РО 4 + 5NO.
Общие способы получения неметаллов
Некоторые неметаллы встречаются в природе в свободном состоянии: это сера, кислород, азот, благородные газы. В первую очередь простые вещества - неметаллы входят в состав воздуха.
Большие количества газообразных кислорода и азота получают ректификацией воздуха (разделением).
Наиболее активные неметаллы - галогены - получают электролизом расплавов или растворов из соединений. В промышленности с помощью электролиза в больших количествах получают одновременно три важнейших продукта: ближайший аналог фтора - хлор, водород и гидроксид натрия. В качестве электролита используют раствор хлорида натрия, подаваемый в электролизер сверху.
Более подробно способы получения неметаллов будут рассмотрены далее, в соответствующих лекциях.
Химические свойства металлов
- Металлы реагируют с неметаллами.
- Металлы, стоящие до водорода, реагируют с кислотами (кроме азотной и серной конц.) с выделением водорода
- Активные металлы реагируют с водой с образованием щелочи и выделением водорода.
- Металлы средней активности реагируют с водой при нагревании, образуя оксид металла и водород.
- Металлы, стоящие после водорода, с водой и растворами кислот (кроме азотной и серной конц.) не реагируют
- Более активные металлы вытесняют менее активные из растворов их солей.
- Галогены реагируют с водой и раствором щелочи.
- Активные галогены (кроме фтора) вытесняют менее активные галогены из растворов их солей.
- Галогены не реагируют с кислородом.
- Амфотерные металлы (Al, Be, Zn) реагируют с растворами щелочей и кислот.
- Магний реагирует с углекислым газом и оксидом кремния.
- Щелочные металлы (кроме лития) с кислородом образуют пероксиды.
Химические свойства неметаллов
- Неметаллы реагируют с металлами и друг с другом.
- Из неметаллов с водой реагируют только наиболее активные – фтор, хлор, бром и йод.
- Фтор, хлор, бром и йод реагируют со щелочами по той же схеме, что и с водой, только образуются не кислоты, а их соли, и реакции не обратимы, а протекают до конца.

Изучай химические свойства
Химические
свойства неметаллов
В соответствии с численными
значениями относительных электроотрицательностей окислительные способности неметаллов
увеличивается
в следующем порядке: Si, B, H, P, C, S, I, N, Cl,
O, F.
Неметаллы как окислители
Окислительные свойства неметаллов
проявляются при их взаимодействии:
· с металлами: 2Na + Cl 2 = 2NaCl;
· с водородом: H 2 + F 2 = 2HF;
· с неметаллами, которые имеют более низкую электроотрицательность: 2Р + 5S = Р 2 S 5 ;
· с некоторыми сложными веществами: 4NH 3 + 5O 2 = 4NO + 6H 2 O,
2FeCl 2 + Cl 2 = 2 FeCl 3 .
Неметаллы как восстановители1. Все неметаллы (кроме фтора) проявляют восстановительные свойства при взаимодействии с кислородом:
S + O 2 = SO 2 , 2H 2 + O 2 = 2H 2 О.
Кислород в соединении с фтором может проявлять и положительную степень окисления, т. е. являться восстановителем. Все остальные неметаллы проявляют восстановительные свойства. Так, например, хлор непосредственно с кислородом не соединяется, но косвенным путем можно получить его оксиды (Cl 2 O, ClO 2 , Cl 2 O 2), в которых хлор проявляет положительную степень окисления. Азот при высокой температуре непосредственно соединяется с кислородом и проявляет восстановительные свойства. Еще легче с кислородом реагирует сера.
2. Многие неметаллы проявляют восстановительные свойства при взаимодействии со сложными веществами:
ZnO + C = Zn + CO, S + 6HNO 3 конц = H 2 SO 4 + 6NO 2 + 2H 2 О .
3. Существуют и такие реакции, в которых один и тот же неметалл является одновременно и окислителем и восстановителем:
Cl 2 + H 2 О = HCl + HClO.
4. Фтор ― самый типичный неметалл, которому нехарактерны восстановительные свойства, т. е. способность отдавать электроны в химических реакциях.
Соединения неметалловНеметаллы могут образовывать соединения с разными внутримолекулярными связями.
Виды соединений неметаллов
Общие формулы водородных соединений по группам периодической системы химических элементов приведены в таблицe :
|
RH 2 |
RH 3 |
RH 4 |
RH 3 |
H 2 R |
||
|
Нелетучие водородные соединения
|
Летучие водородные соединения
|
|||||
С кислородом неметаллы образуют кислотные оксиды. В одних оксидах они проявляют максимальную степень окисления, равную номеру группы (например, SO 2 , N 2 O 5), а других ― более низкую (например, SO 2 , N 2 O 3). Кислотным оксидам соответствуют кислоты, причем из двух кислородных кислот одного неметалла сильнее та, в которой он проявляет более высокую степень окисления. Например, азотная кислота HNO 3 сильнее азотистой HNO 2 , а серная кислота H 2 SO 4 сильнее сернистой H 2 SO 3 .
Характеристики кислородных соединений неметаллов
1. Свойства высших оксидов (т. е. оксидов, в состав которых входит элемент данной группы с высшей степенью окисления) в периодах слева направо постепенно изменяются от основных к кислотным.
2. В группах сверху вниз кислотные свойства высших оксидов постепенно ослабевают. Об этом можно судить по свойствам кислот, соответствующих этим оксидам.
3. Возрастание кислотных свойств высших оксидов соответствующих элементов в периодах слева направо объясняется постепенным возрастанием положительного заряда ионов этих элементов.
4. В главных подгруппах периодической системы химических элементов в направлении сверху вниз кислотные свойства высших оксидов неметаллов уменьшаются.